Ραδιενεργό Ιώδιο & Καρκίνος Θυρεοειδούς
Τι είναι το ραδιενεργό ιώδιο;
Το ραδιενεργό ιώδιο αποτελεί τη ραδιενεργό μορφή του ιωδίου που παράγεται τεχνητά από το ιώδιο που υπάρχει σε αφθονία στη φύση. Τις τελευταίες δεκαετίες, το ραδιενεργό ιώδιο αποτελεί μία θεραπεία της πυρηνικής ιατρικής.
Υπάρχουν δύο τύποι ραδιενεργού ιωδίου διαθέσιμοι σήμερα:
- Το ραδιενεργό ιώδιο – 123 (Ι-123)
- Το ραδιενεργό ιώδιο – 131 (Ι-131)
Το Ι-123 χρησιμοποιείται μόνο για διαγνωστικούς σκοπούς, καθώς δεν έχει τη δυνατότητα καταστροφής των κυττάρων-στόχων. Αντιθέτως, το Ι-131 μπορεί να χρησιμοποιηθεί τόσο διαγνωστικά όσο και θεραπευτικά, με τη χορήγησή του να βρίσκει, συνήθως, εφαρμογή στον θεραπευτικό τομέα.
Πως σχετίζεται το ραδιενεργό ιώδιο με το θυρεοειδή αδένα και τον καρκίνο θυρεοειδούς;
Το ιώδιο είναι εξαιρετικά απαραίτητο στο θυρεοειδή αδένα για τη σύνθεση των θυρεοειδικών ορμονών, δηλαδή της Τ3 και της Τ4. Εξαιτίας αυτής της σχέσης εξάρτησης του θυρεοειδούς με το ιώδιο για τη σύνθεση των ορμονών, το ραδιενεργό ιώδιο μπορεί και απορροφάται από τον θυρεοειδή και ως εκ τούτου προκαλεί την καταστροφή των κυττάρων του θυρεοειδούς. Αυτό ισχύει και για τον καρκίνο θυρεοειδούς, ο οποίος εμφανίζει εξαιρετικά αυξημένο ρυθμό πολλαπλασιασμού και ως εκ τούτου οι ανάγκες του σε ιώδιο είναι αυξημένες.
Συνεπεία της υψηλής συγγένειάς του με το θυρεοειδή αδένα και τα κύτταρά του, η χορήγηση ραδιενεργού ιωδίου – 131 προκαλεί την καταστροφή μόνο αυτών των κυττάρων και όχι άλλων κυττάρων του οργανισμού. Για το λόγο αυτό, η χορήγησή του εφαρμόστηκε στο παρελθόν στη θεραπεία διαφόρων παθήσεων του θυρεοειδούς, όπως η βρογχοκήλη.
Κατά παρόμοιο τρόπο, τα κύτταρα των καλώς διαφοροποιημένων καρκίνων θυρεοειδούς (θηλώδης, θυλακιώδης και καρκίνος Hürthle) καταστρέφονται, επίσης, σε άλλοτε άλλο βαθμό από το ραδιενεργό ιώδιο – 131. Αυτό, βέβαια, δεν ισχύει για το μυελοειδή καρκίνο θυρεοειδούς, καθώς προέρχεται από τα παραθυλακιώδη κύτταρα (κύτταρα C) του θυρεοειδούς και όχι από τα θυρεοειδικά κύτταρα.
Ποια είναι η αποτελεσματικότητα του ραδιενεργού ιωδίου και ποια τα οφέλη του για τους ασθενείς με καρκίνο θυρεοειδούς;
Πολυάριθμες επιστημονικές έρευνες έχουν εξετάσει την αποτελεσματικότητα του ραδιενεργού ιωδίου στην καταστροφή των κυττάρων των καλώς διαφοροποιημένων καρκίνων θυρεοειδούς. Κοινός παρονομαστής των ερευνών αυτών είναι πως το ραδιενεργό ιώδιο – 131 εμφανίζει αποτελεσματικότητα στην πλήρη καταστροφή των κυττάρων των καλώς διαφοροποιημένων καρκίνων θυρεοειδούς της τάξεως του 70 – 100%.
Η καταστροφή των μη ορατών δια γυμνού οφθαλμού υπολειμμάτων καρκίνου του θυρεοειδούς από τη χορήγηση του Ι-131 μόνο ευεργετική μπορεί να χαρακτηριστεί, καθώς συμβάλλει στην επίτευξη οριστικής ίασης των ασθενών αυτών και ταυτόχρονα στην ελαχιστοποίηση ενδεχόμενης υποτροπής της νόσου.
Ωστόσο, η χορήγηση του ραδιενεργού ιωδίου δεν είναι πανάκεια και θα πρέπει να εξατομικεύεται, με βάση συγκεκριμένες ενδείξεις, οι περισσότερες εκ των οποίων προκύπτουν από την ιστολογική εξέταση (βιοψία) του αφαιρεθέντος θυρεοειδούς αδένα. Ως εκ τούτου, γεννάται το ερώτημα της ωφέλειας των ασθενών με καρκίνο θυρεοειδούς χαμηλής επικινδυνότητας από τη μετεγχειρητική χορήγησή του.
Η επιστημονική έρευνα
Την απάντηση στο ερώτημα του οφέλους των ασθενών με καρκίνο θυρεοειδούς χαμηλής επικινδυνότητας από τη μετεγχειρητική χορήγηση ραδιενεργού ιωδίου έρχεται να δώσει μία έρευνα που δημοσιεύθηκε στο πλέον έγκριτο παγκοσμίως επιστημονικό ιατρικό περιοδικό “The New England Journal of Medicine“.
Η έρευνα συνέκρινε την αποτελεσματικότητα του ραδιενεργού ιωδίου – 131 στην ελαχιστοποίηση της δομικής και λειτουργικής υποτροπής της νόσου, σε σχέση με τη μη χορήγηση ραδιενεργού ιωδίου.
Μόνο ενήλικες ασθενείς με καλώς διαφοροποιημένο καρκίνο θυρεοειδούς χαμηλής επικινδυνότητας (θηλώδης, θυλακιώδης ή καρκίνος Hürthle) που είχαν υποβληθεί σε ολική θυρεοειδεκτομή συμπεριλήφθησαν στη μελέτη, με τα στάδια της νόσου τους να είναι:
- T1: καρκίνος θυρεοειδούς ≤ 2 εκ. στη μέγιστη διάμετρό του &
- Ν0: απουσία παθολογικών λεμφαδένων τόσο κλινικά όσο και στην ιστολογική εξέταση.
- Απουσία επιθετικών ιστολογικών υποτύπων
Οι ασθενείς, λοιπόν, που έλαβαν ραδιενεργό ιώδιο – 131 υπεβλήθησαν στη θεραπεία μετά τη χορήγηση συνθετικής θυρεοτροπίνης (TSH), με στόχο την αύξηση της αποτελεσματικότητας της θεραπείας. Η συνολική δόση ραδιενέργειας σε κάθε ασθενή ήταν 30mCi. Αντιθέτως, οι ασθενείς που δεν έλαβαν τη θεραπεία υπεβλήθησαν μόνο σε ολική θυρεοειδεκτομή.
Συνολικά, 363 ασθενείς έλαβαν μετεγχειρητική θεραπεία με ραδιενεργό ιώδιο – 131 και συγκρίθηκαν με 367 ασθενείς που δεν έλαβαν ραδιενεργό ιώδιο.
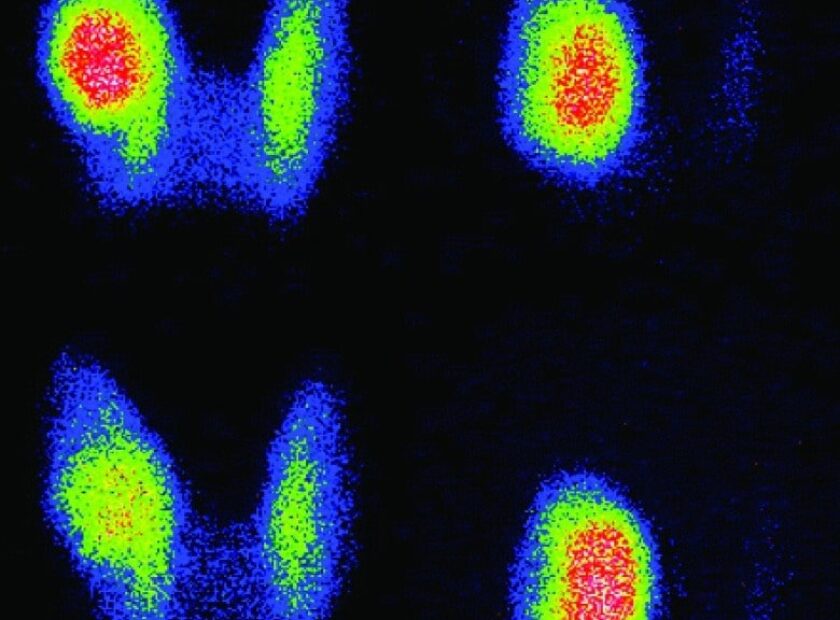
Η παρακολούθηση όλων των ασθενών ήταν για ένα χρονικό διάστημα 3 ετών μετά τη θεραπεία τους. Ενδεχόμενη δομική υποτροπή της νόσου ανιχνεύθηκε μέσω του υπερηχογραφήματος και του σπινθηρογραφήματος με ραδιενεργό ιώδιο, ενώ η λειτουργική υποτροπή της νόσου μέσω της μέτρησης των επιπέδων θυρεοσφαιρίνης αίματος.
Τα ευρήματα της έρευνας
Η έρευνα, λοιπόν, αποκάλυψε πως η συμπληρωματική χορήγηση ραδιενεργού ιωδίου – 131 στους ασθενείς με καλώς διαφοροποιημένους καρκίνους θυρεοειδούς χαμηλής επικινδυνότητας δεν προσφέρει κάποιο πλεονέκτημα έναντι της μη χορήγησης του, όσον αφορά στην υποτροπή της νόσου, ακόμη και μετά από 3 έτη παρακολούθησης.
Πιο συγκεκριμένα, ανιχνεύθηκαν 15 υποτροπές (4.1%) έναντι 16 υποτροπών (4.4%) της νόσου, στους ασθενείς που έλαβαν ραδιενεργό ιώδιο, σε σύγκριση με εκείνους που δεν το έλαβαν, αντίστοιχα. Το εύρημα αυτό υποδεικνύει πως στατιστικά και ουσιαστικά, η συμπληρωματική χορήγηση ιωδίου δεν προσέφερε ουσιαστικά κάποιο πλεονέκτημα στους ασθενείς που το έλαβαν.
Επιπρόσθετα, η έρευνα αποκάλυψε πως ο κίνδυνος υποτροπής της νόσου ήταν ανεξάρτητος της χορήγησης ή μη ραδιενεργού ιωδίου, με τους κύριους παράγοντες κινδύνου για υποτροπή να είναι:
- Καρκίνος θυρεοειδούς μεγέθους ≤ 14 χιλιοστών &
- Αυξημένα μετεγχειρητικά και μεταθεραπευτικά επίπεδα θυρεοσφαιρίνης αίματος.
Συμπεράσματα
Συμπερασματικά, η χορήγηση ραδιενεργού ιωδίου αποτελεί ένα εξαιρετικά αποτελεσματικό συμπληρωματικό θεραπευτικό μέσο της χειρουργικής θεραπείας σε ασθενείς με καρκίνο θυρεοειδούς που πληρούν συγκεκριμένες ενδείξεις.
Ωστόσο, η χρήση του θα πρέπει να εξατομικεύεται και δεν θα πρέπει να αποτελεί πανάκεια, ειδικότερα σε ασθενείς με καλώς διαφοροποιημένους χαμηλής επικινδυνότητας καρκίνους θυρεοειδούς.
Οι ασθενείς αυτοί αποδείχθηκε πως δεν ωφελούνται ουσιαστικά από τη θεραπεία αυτή και θα πρέπει να παρακολουθούνται στενά μετεγχειρητικά, όπως όλοι οι ασθενείς με καρκίνο θυρεοειδούς. Σε ενδεχόμενη υποτροπή της νόσου τους, η χορήγηση ιωδίου θα συμβάλλει καθοριστικά στον εκ νέου έλεγχο της νόσου, αποτρέποντας έτσι μια πιθανή επανεπέμβαση στην περιοχή του τραχήλου, η οποία συνοδεύεται από αυξημένα ποσοστά νοσηρότητας, συγκριτικά με τις πρωτογενείς χειρουργικές επεμβάσεις.

Ο εξειδικευμένος χειρουργός Δρ. Κωνσταντίνος Αποστόλου, είναι στη διάθεσή σας για να απαντήσει και να λύσει κάθε απορία σας. Μην διστάσετε να επικοινωνήσετε μαζί μας για οτιδήποτε σας απασχολεί.